検査と診断のながれ
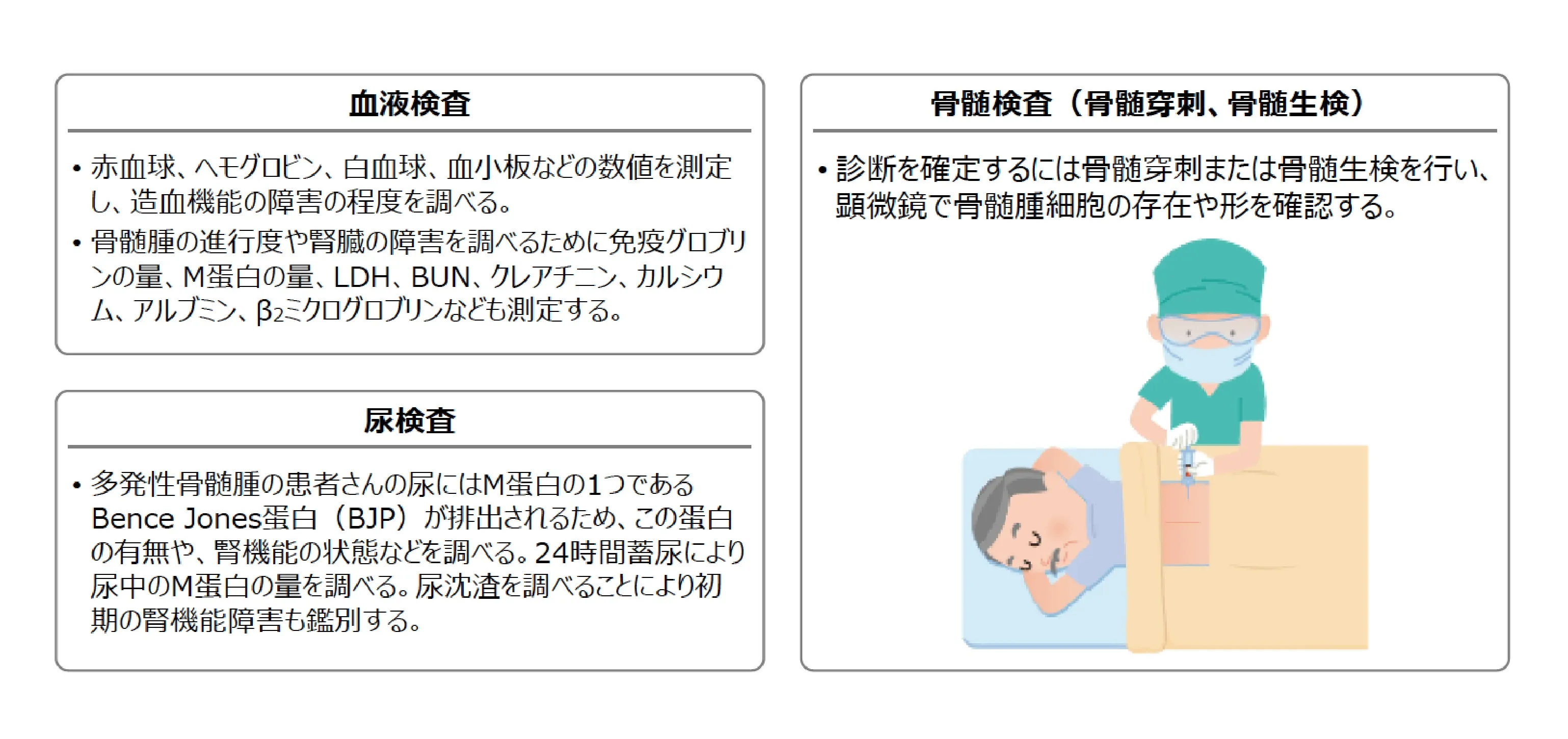
- 多発性骨髄腫が疑われる場合は、血液検査、尿検査、骨髄検査が行われる。
さらに画像検査(骨X線検査やCT検査など)で全身の骨の状態および髄外腫瘤を調べる。
日本臨床検査医学会ガイドライン作成委員会 編. 臨床検査のガイドライン JSLM2021, 2021; 宇宙堂八木書店, 443.
主な検査
- 多発性骨髄腫ではM蛋白が過剰に産生されることから、血液中や尿中のM蛋白の有無を確認する。
また、骨髄腫細胞の増殖による造血機能への影響を確認するため、赤血球数などを確認する。 - M蛋白が検出された場合には、骨髄穿刺により骨髄液を採取して、骨髄腫細胞の有無を確認する。
併せて骨髄生検も施行し骨髄繊維症の有無も調べる。
図 主な検査
飛内賢正 監.血液のがん 悪性リンパ腫・白血病・多発性骨髄腫,2015; 講談社,76
骨髄検査と診断
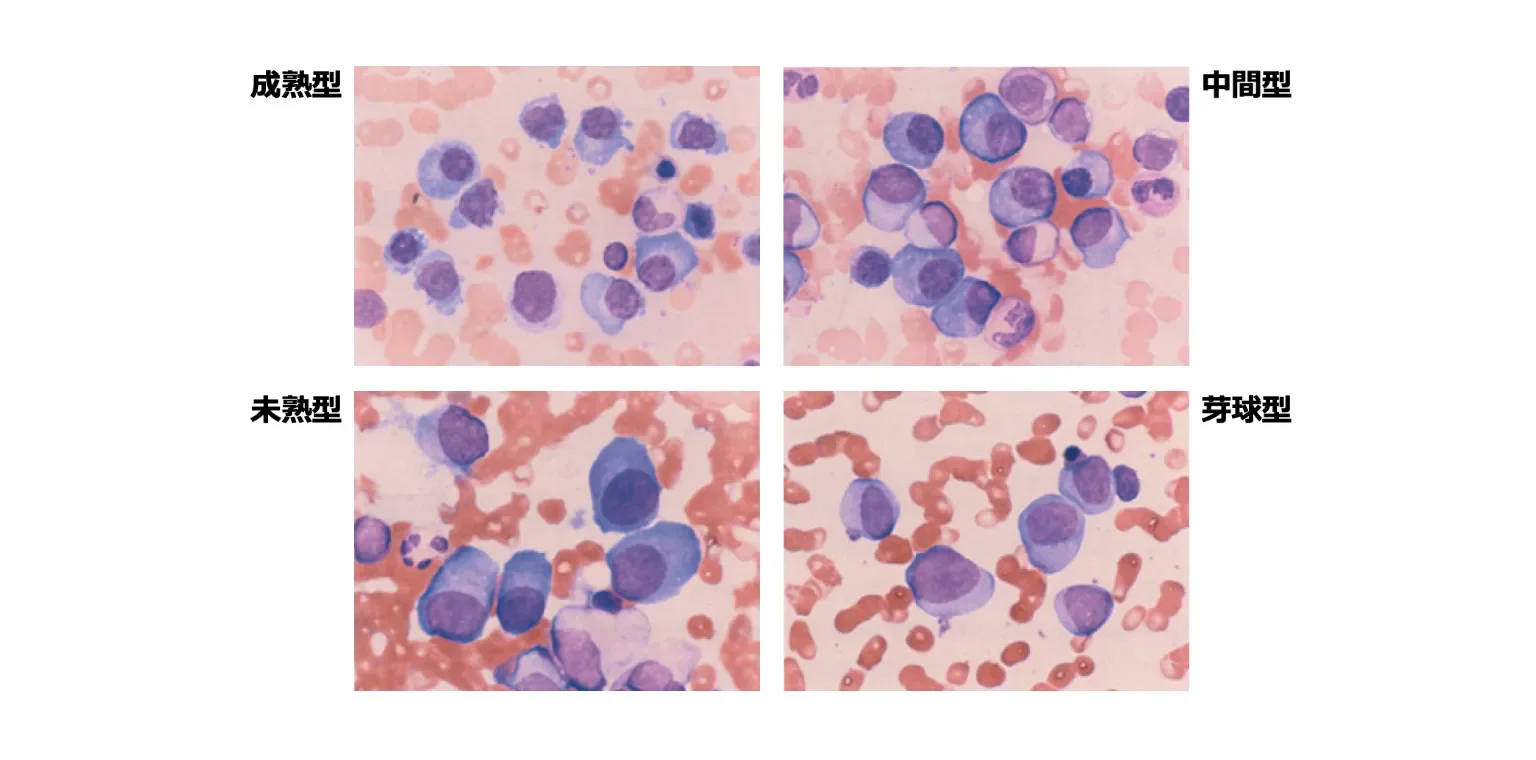
- 多発性骨髄腫の骨髄では、形質細胞の増殖がみられる。
- メイ・ギムザ(May-Giemsa)染色で細胞質が青く染まる。
- 骨髄腫細胞は形態学的に不均一であり、成熟型、中間型、未熟型、芽球型の4型に分類するGreipp分類1)が広く知られている。
図 骨髄腫細胞の形態2)
1)
Greipp PR, et al.: Blood. 1985; 65: 305-310.
2)
堀田知光 編. みんなに役立つ多発性骨髄腫の基礎と臨床, 2008; 医薬ジャーナル社, 90.
細胞表面抗原
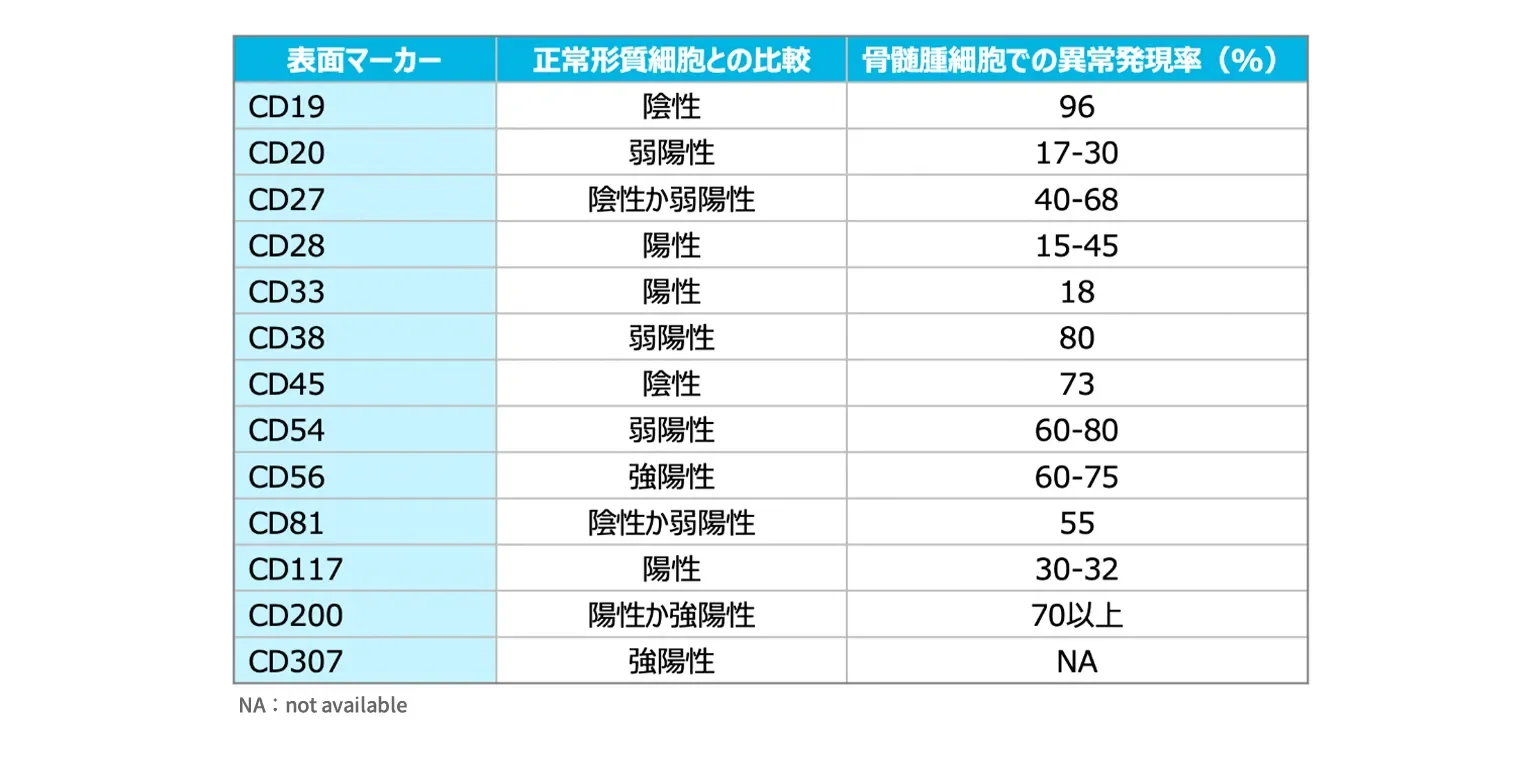
- フローサイトメトリー法を用いて骨髄腫細胞表面にどのような抗原蛋白(表面マーカーともいう)が発現しているかを検索することは、多発性骨髄腫の診断のみならず、予後予測や治療後の微小残存病変 minimal residual disease(MRD)を評価するのに有用である1)。
表 骨髄腫細胞に発現する表面マーカー1,2)
1)
日本骨髄腫学会 編. 多発性骨髄腫の診療指針(第6版), 2024; 文光堂, 15.
2)
Flores-Montero J, et al.: Cytometry B Clin Cytom. 2016; 90: 61-72.
M蛋白の確認
血清蛋白電気泳動-SPEP
- 多発性骨髄腫では骨髄腫細胞によるM蛋白の産生により、単クローン性γグロブリン血症となる。
- 血清蛋白を電気泳動にかけるとM蛋白に相当するγ分画の上昇がみられる。これをMピークという。
河野道生ほか 血液・造血器疾患学 2008; メジカルビュー社 226. より改変
尿蛋白電気泳動-UPEP
- 尿蛋白電気泳動は、Bence Jones蛋白(BJP)の有無を調べ、かつその濃度をモニターするために使用される。
- また、MMでよくみられる合併症の腎障害の評価にも役立つ。
日本血液学会 日本リンパ網内系学会 編 造血器腫瘍取扱い規約(第 1 版) 2010; 金原出版 170. より改変
M蛋白の検査
免疫電気泳動法-IEP
- 免疫電気泳動法は、定性的分析法で、血清や尿中のさまざまな蛋白の同定が可能である。
- 沈降線を観察することで、個々の蛋白の異常をみることができる。
抗IgG、IgA、IgM、κ、λ血清を使用することで、M蛋白の種類が同定される。
図 免疫電気泳動法1)
1)
末永孝生ほか.多発性骨髄腫 Updating(第1巻), 2012; 医薬ジャーナル社, 155.
免疫固定法-IFE
- 抗原抗体反応により免疫沈降物を染色し検出する。M蛋白が拡散せずに固定化することが可能で、微量なM蛋白の検出に有用である。
末永孝生 ほか. 多発性骨髄腫 Updating(第1巻), 2012; 医薬ジャーナル社, 155.
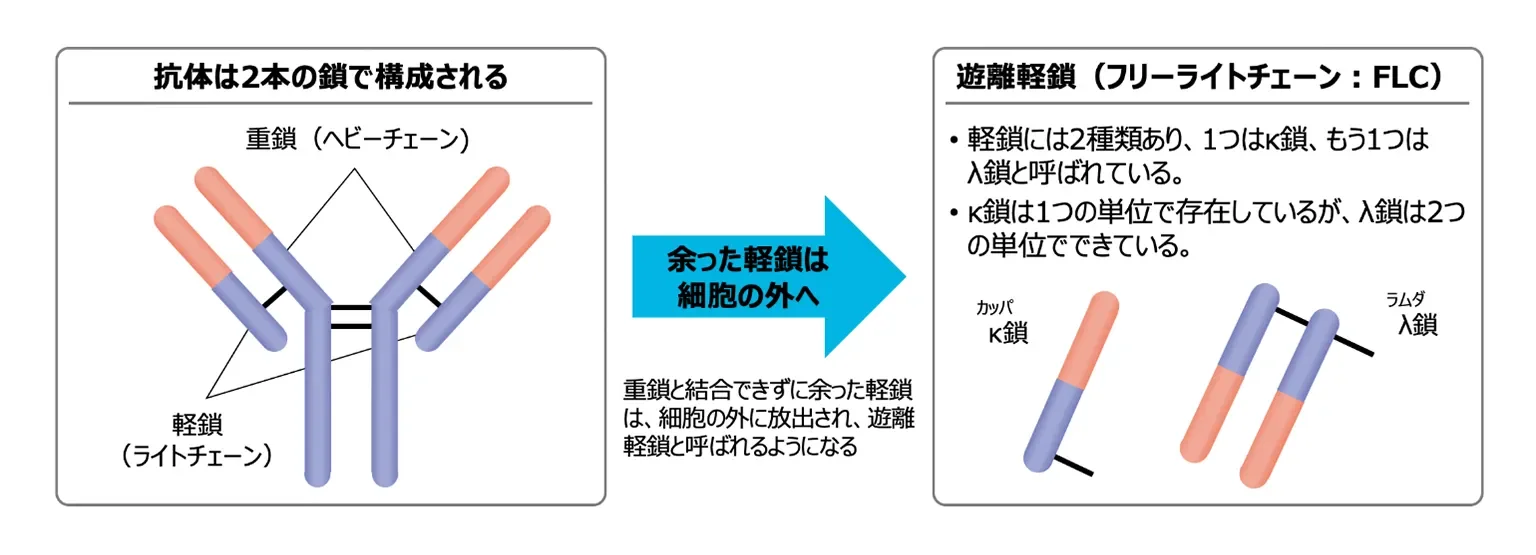
血清遊離軽鎖測定法(sFLC検査)
- sFLC検査は、M蛋白の検出感度が高く、形質細胞性疾患のスクリーニング検査としては、血清蛋白電気泳動、免疫固定法とともに必須の検査である1)。この測定法は正常域のFLCの測定が可能で、微量のM蛋白の検出も可能である2)。
- sFLC(κ鎖/λ鎖)比の異常は、形質細胞増殖性疾患の予後因子として重要である1)。
- 測定可能病変の有無にかかわらず、sFLC測定は迅速な治療奏効の判断と再発の初期兆候を知る上で有用であり、また、sFLC κ/λ比の正常化は、sCRの判定にも必要である1)。
図 抗体の基本構造
1)
日本骨髄腫学会 編. 多発性骨髄腫の診療指針(第6版), 2024; 文光堂, 11.
2)
Dispenzieri A, et al.: Leukemia. 2009; 23: 215-224.
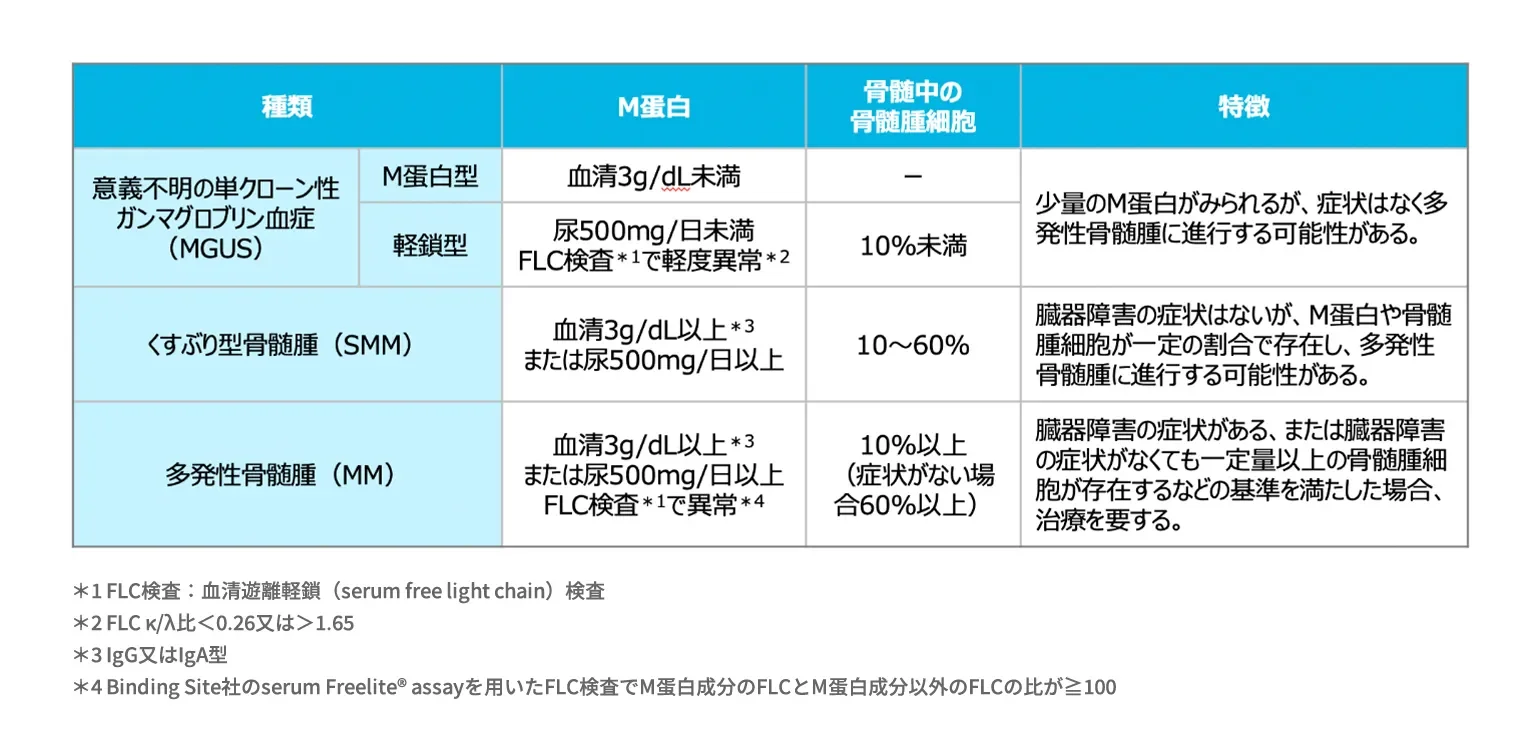
診断基準-症候性多発性骨髄腫
多発性骨髄腫の診断基準(IMWG、2014改訂) 1、2)
多発性骨髄腫の定義
以下の2項目を満たす。
① 骨髄のクローナルな形質細胞割合≧10%、または生検で確認された骨もしくは髄外形質細胞腫を認める*1。
② 以下に示す骨髄腫診断事象の1項目以上を満たす。
骨髄腫診断事象(MDE)
◉ 形質細胞腫瘍に関連した臓器障害
- 高カルシウム血症:血清カルシウム>11mg/dLもしくは正常値上限より1mg/dLを超えて高い
- 腎障害:クレアチニンクリアランス<40mL/分*2もしくは血清クレアチニン>2mg/dL
- 貧血:ヘモグロビン<10g/dLもしくは正常値下限より2g/dLを超えて低い
- 骨病変:全身骨単純X線写真、CTもしくはPET-CTで溶骨性骨病変を1ヵ所以上認める*3
◉ 進行するリスクが高いバイオマーカー(SLiM)
- 骨髄のクローナルな形質細胞割合≧60%
- 血清遊離軽鎖(血清FLC)比(M蛋白成分のFLCとM蛋白成分以外のFLCの比)≧100*4
- MRIで局所性の骨病変(径5mm以上)>1ヵ所
*1:
クロナリティーは、フローサイトメトリー、免疫組織化学ないし免疫蛍光法でκ/λ比の偏りを証明することが必要である。
*2:
実測するか、推定式(modification of diet in renal disease[MDRD]、またはchronic kidney disease epidemiology collaboration[CKD-EPI]の計算式)を用いる。
*3:
骨髄中形質細胞比率が10%未満の場合は、孤発性形質細胞腫との鑑別のために2個以上の溶骨性病変が必要である。
*4:
評価にはBinding Site社のserum Freelite® assayを用いる。またFLC≧100mg/Lが必要である。
1)
Rajkumar SV, et al.: Lancet Oncol. 2014; 15: e538-548.より引用
2)
日本骨髄腫学会 編. 多発性骨髄腫の診療指針(第6版),2024;文光堂,26.
MMへの進展

表 症候性骨髄腫患者の初診時主訴1)
1)
Rajkumar SV, et al.: Lancet Oncol. 2014; 15: e538-548.より作成
病期分類
- 1975年よりDurie & Salmon分類が広く用いられてきたが、最近では予後に関連しないためあまり用いられない。
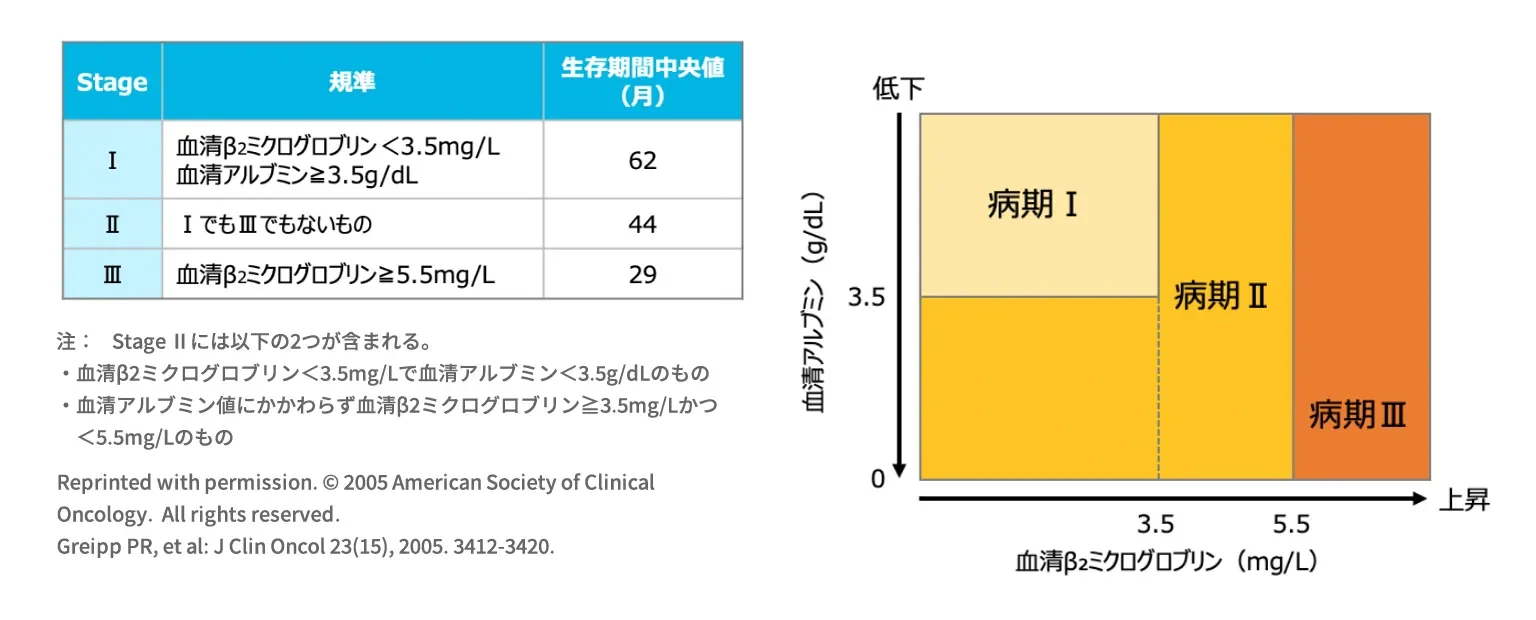
- 国際骨髄腫ワーキンググループ(IMWG)により病期分類には国際病期分類(ISS)が作成された。
- また、ISS分類に血清乳酸脱水素酵素(LDH)の検査値と、特定の染色体異常を組み合わせたRevised ISS分類(R-ISS分類)が提唱された。
図 International Staging System1)
1)
Greipp PR, et al.: J Clin Oncol. 2005; 23: 3412-3420.
2025年5月作成
承認番号:2003-JP-250001010